食品 运行与管理
----研究型与检测类 管理规范
检测类 严格按CNAS17025和CMA、CMAF要求进行管理,于2014年底通过了国家认监委组织的 评审,并于2016年4月通过了 的监督、扩项评审。目前,理化室分为常规理化检测、光谱检测、色谱-质谱检测和微生物 ,本文主要介绍本 的运行和管理。
据集团和研究院的研发需求和食品安全管理需求,开发与食品安全和食品品质检测相关的分析技术,服务集团的业务单元和二级、三级检测体系。下面,从环境条件、人员、仪器、信息、体系等方面进行介绍。
环境
建设布局
集团检测中心 选址在昌平北七家镇未来科技城,远离生活区和交通枢纽的安静场所。在 建设时注重采光充足,通风良好,水、电供应充足,气路、排风、下水路布局合理畅通。检测中心 总面积7000 m2。在检测中心建设布局上分为样品储存室、办公室和 。 分为微生物 和理化 两大部分。依据检测方法和仪器使用情况,理化 又分为色谱—质谱 (以有机分析为主,涉及农药残留、兽药残留、食品添加剂、营养成分及组成分析)、光谱 (以金属元素为主,还包括:分子光谱)和常规理化 三部分。 总体布局和各科室布局符合实验流程,尽量减少往返迂回,减少污染,方便操作。
各科室实验区域和非实验区域隔开,降低潜在危害;安全设施齐备,每房间放置灭火器,区域设置淋洗器、洗眼器和急救药箱。理化 要求恒温恒湿,设置标准溶液配制间、天平间(万分之一和十万分之一的精密天平,需要设置缓冲区)、试剂间、洗刷室(或洗刷区域)。理化 中的光谱、色谱 仪器操作间和前处理室隔开,常规理化 设置感官 。
.jpg)
水电气路
用水:保证充足的 用水和消防用水。下水路排水通畅,尽可能减少拐弯,并在拐弯处预留清理孔。酸性废水或碱性废水中和后排放。废弃的有机溶剂和固体废弃物集中收集由专门机构回收处理。
用电:计算 内使用仪器的总功率,保证用电充足。满足特殊仪器电压需求,如同位素质谱需380伏电压。每个房间布有三相交流电和单项交流电,配置总电源开关,实验台和墙电插座分布合理。
气路: 气室设置于一层,统一供应。气路共分9路:普氮、高纯氮、空气、高纯氦气、氢气、氩气、乙炔气等。
通风: 每小时换风5次,保证室内的温度、湿度、新风补充和洁净度。
废液:由专门公司统一回收处理。
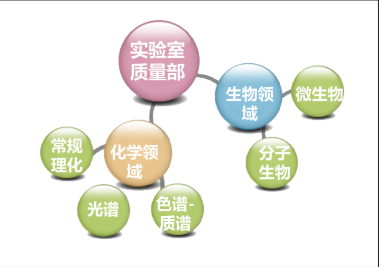
关键岗位划分
环境内务
依据GB/T20000.1-2002《标准化工作指南 标准化和相关活动的通用词汇》施行标准化管理。 各区域 规章制度上墙,明确实验须知。各房间设置房间牌、警示标示(生化标识、辐射标识)。柜和抽屉贴有目录标签。
各区域 装有出入门禁,进入工作区域时必须穿戴整洁的实验服。禁止将与实验无关的物品带入工作区域。严禁在工作区域进行餐饮、吸烟等危险活动。
实验中必须配备个人防护设施,如护目镜、口罩、手套等,实验中禁止佩戴隐形眼镜。
各实验相关房间配置温湿度记录仪、冰箱配置温度计,每日填写房间温湿度记录表和冰箱温度记录表。每日 封闭前检查仪器、水电、气路、通风等环境安全,并填写巡检记录表。
人员
人员配置
人员配置:为保障 稳定运转,各关键岗位实行双岗制。岗位共涉及2个领域,5个重点岗位。 目前共有检测人员52名。
管理层: 主任1人,院分析检测副总工程师担任技术负责人1人, 主任兼质量负责人。质量部4人,色谱组18人,光谱组8人,常规理化组8人,微生物组(含分子生物)10人。
另设岗位:文件资料管理员、样品管理员、内审员、质量监督员等(均为兼职)。
人员管理
人员人工,按质量手册和17025体系,由质量负责人负责体系运行,技术负责人负责检测活动。明确人员岗位职责,明确人员检测领域、检测项目范围和仪器使用范围,持证上岗。
建立人员档案记录、人员转正考评记录、人员日常监督记录、人员实验项目培训记录等档案记录。 定期对 人员进行实验培训,提高检测能力。
物资
仪器
仪器设备我们主要按照ISO/IEO 17025中5.5节规定、GB/T27404-2008 《 质量控制规范食品理化检测》 附录B 以及量值溯源管理程序进行设备管理和计量。检测设备均由计量院进行计量,贴有运行状态标识。仪器管理分配到人,设备编号标签唯一。建立设备档案台账、设备使用授权表、仪器使用保养记录、仪器期间核查记录、仪器标准操作规程等档案记录。脱离 直接控制(如,搬家移动)的设备在恢复使用前须有核查记录。仪器陈列做到分类、定室、定柜、定点, 做到防尘、防腐、防震(尤其天平)。钢瓶、气瓶入柜上锁。
计量器具
依据JJG 196-2006《玻璃量器检定规程》对玻璃量器进行使用和计量。实验中使用的A级计量器具包括移液管、容量瓶、移液枪等均由计量院计 量检定,贴有检定标识。带刻度的滴管、带刻度的试管、带刻度的离心管、进样瓶等不属于计量器具,不可以用于定容。
样品
样品的抽样、制备与储存主要参照GB/T27404-2008 附录E的要求。样品信息要求体现完整、准确,样品编号唯一。建立样品采样记录、样品登记记录、样品领取记录、样品储存销毁记录、冰箱冰柜温度记录等档案记录。
.jpg)
试剂
试剂按照类别分类存放,存放场所避免阳光直射,温度适宜。试剂来源可靠,质量、纯度合格,不过期,不过多储存(尤易燃易爆试剂)。试剂柜贴签,由专人负责管理,建立索引目录、试剂信息记录、试剂领用记录等档案记录,要求定期核对。易制毒试剂依据《易制毒化学品管理规范》管理,建立有出入库及使用领取记录。易制毒试剂如:三氯甲烷、乙醚、甲苯、丙酮、苯乙酸等。剧毒试剂管理设置保险柜或保险库,要求双人双锁。剧毒试剂如三氧化二砷、叠氮钠等。易潮解试剂置于干燥器保存。配置的试剂注明试剂成分名称、配置日期、配置人。
.jpg)
标品
标准品按照储存温度分为常温、冷藏、冷冻储存。储存过程中又按照标准品类别分区域存放,由专人负责管理。建立索引目录、标品信息记录、标品领用记录、标品配置记录、标品期间核查记录等档案记录且对标品证书进行统一管理。标准滴定溶液依据GB/T601-2002《化学试剂 标准滴定溶液的制备》在标准溶液配置间配置。实验用水依据GB/T6682-2008 《分析 用水规格和试验方法》要求。标准溶液储存条件及有效期等信息,主要参照:GB/T27404-2008附录C。
信息
文件资料
质量体系文件有唯一性标识。标识包括:发布日期、修订标识、页码、总页数、发布机构、文件结束标记。
建立文件储存归档程序:如,人员档案、仪器标品档案、程序文件档案、原始记录和留底报告等。某些资料为方便管理,允许记录储存于硬盘、光盘等电子媒体上,设置加密并由专人负责登统修改。(依据ISO/IEO17025中4.12.1.2规定)
建立文件控制程序:规章、标准、报告纸张、原始记录纸张、 出现的纸质版标准等文件都要有受控章、发放号、发放记录。 内不准出现不受控的文件,不可随意打印检测标准。(依据ISO/IEO17025中4.3.2规定)
建立文件变更程序。如质量文件的修改的新的内容在附录中标明,在再版之前只允许手写修改。又如原始记录的修改处双划线、签名缩写首字母并标注日期。一份原始记录的更改一般不多于2处。(依据ISO/IEO17025中4.3.3规定)
检测方法
无论是应用检测标准还是非标方法,首次开展的实验项目需要做该项目的方法学验证报告;方法学验证报告的参数要求按照GB/T27404-2008 附录F的要求;
方法成熟应用后编写方法标准操作程序文件(检验方法的SOP文件);
对应用的检测方法进行不确定度评定(依据ISO/IEO 17025中5.4.6规定);
在选择项目的检验方法时考虑样品属性、产品标准、产品用途等因素。

记录报告
原始记录和检测报告实行双三级审核。原始记录完成后由实验员签字,同组其他实验员校对签字,各组技术负责人审核签字。检测报告由报告编制人、报告审核人、本领域的批准人分别审核签字。所有检测工作都应有原始记录。原始记录完整,体现一系列量值传递信息,数据准确,附有仪器谱图。数据结果经过校准与复核。检测报告信息完整,包括样品基本信息、协议书信息、检测结果、方法依据等关键信息。检测报告复印版同原始记录合并后留底存档。
LIMS
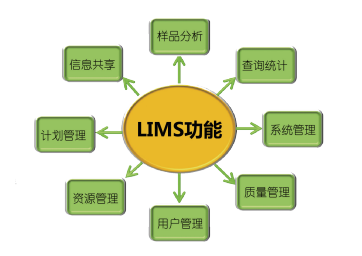
正在建设中的 信息管理系统(LIMS)将完成 数据和信息的收集、分析、报告和管理,并且通过此信息平台实现全集团 数据联网,系统将于年底正式运行。以 为中心,将 的业务流程、 环境、人员、仪器设备、标物标液、化学试剂、标准方法、文件记录、科研管理、项目管理等因素进行有机结合,实现数据网上调度、数据自动采集、快速分布、信息共享。
体系
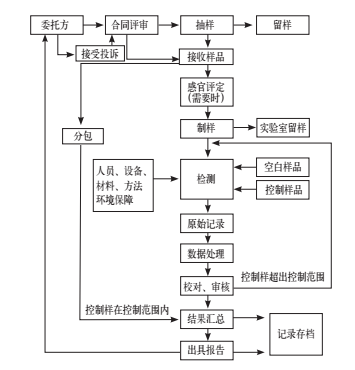
检测流程
在 检测流程上,我们参考的是GB/T 27404-2008 附录D规定。
体系程序
体系程序,依据ISO/IEO17025要求,主要注意以下几项:
是否建立了质量体系(包括:管理结构框架、政策制度、计划、程序指导书等)、质量方针声明、总体目标、执行质量文件程序等。
管理体系是否覆盖到了临时工作环境,如抽样过程,采样过程。
是否建立了文件控制程序和文件变更程序。
是否建立合同评审程序,合同评审还要包括外包任务的评审。
是否有服务和供应品采购程序,如试剂耗材、标品购买、验收和存储的程序。
是否已建立客户服务和投诉程序。
是否已建立改进程序、纠正措施和预防措施。预防措施:例如实施充分监督、样品的复检程序、员工的技能培训、标准品的期间核查、仪器的期间核查等。
是否已建立内部审核和管理评审程序。频率一年一次。
本文作者来自中粮营养健康研究院。
展源
何发
相关文章
-

QC, IQC, IPQC, QA,到底是什么鬼?
2020-05-27
-

AAS法分析茶叶中的铅,镉,砷
2020-05-27
-
LIMS仪器接口在 自动化管理中的应用
2020-05-27
-
红外光谱分析,你了解多少?
2021-01-11
-

超净工作台原理,使用与维护
2020-05-27
-

三聚氰胺,你还要害多少人
2020-05-27
-

HPLC检测器,你了解吗?
2024-03-06
-

选对 ,快速开发方法
2020-05-27
-

关注面向未来的 生态系统及全生命周期, 助力中国下一代 规划与建设
2020-05-27
-

食品 的LIMS系统
2020-05-27

加载更多