高分辨率质谱技术在高质荷比离子分析方面的进展
高分辨率质谱
现代质谱(MS)面临的一个主要挑战是如何在高质荷比(m/z)区域实现高质量分辨率和高精度的分析。为了提高MS的实际应用能力,了解最新技术的局限性及其在应用科学中的地位至关重要。本综述总结了高分辨质谱(HRMS)中的重要仪器和相关的研究进展,这些仪器的前沿研究将其工作范围扩展到高m/z区域。
高分辨质谱
(HRMS)
在现代分析科学中具有不可或缺的作用,因为它具有精确识别未知化合物和定量样品中待测化合物的优越性能。
质量分辨率
(MRP)
、质量准确度、灵敏度和适用的质量范围是决定质谱仪性能最重要的属性。
MRP
是量化离子峰锐度的因子,人们将其定义为观察到的质量
(m)
与最大峰高的特定分数之比,在谱图中通常用质谱离子峰的半峰宽
(FWHM)
高度或
δm
表示。
具有较高
MRP
的质谱仪可以潜在地分辨更多的特征,因为它可以产生具有较高峰值容量的质谱图。
另一方面,质量精度是指测定的
m/z
与其精确理论值的差值;
质量精度可以代表测量结果的正确性。
高质量精度可通过几个基本要求获得,例如仪器需要具有足够的电子分辨率、高
MRP
、稳定的离子源和稳定的电气系统等。
MS
的灵敏度是高质量应用中的另一个关键问题。
它依赖于合适的样品制备和电离方法,例如电喷雾电离
(ESI)
可以从水溶性样品中产生多电荷分子,基质辅助激光解吸电离
(MALDI)
主要从固体样品中产生单电荷分子。
旨在提高电离效率的研究十分常见,在这里我们鼓励读者查阅相关文献和综述文章。
高分辨率仪器通常被认为是具有提供
10000
以上
MRP
的仪器。
通过使用具有这种
MRP
的质谱仪,人们可以在低
m/z
范围内
(
即
<1000)
实现精确的分子鉴定,但它们不能为大分子分析提供类似的性能。
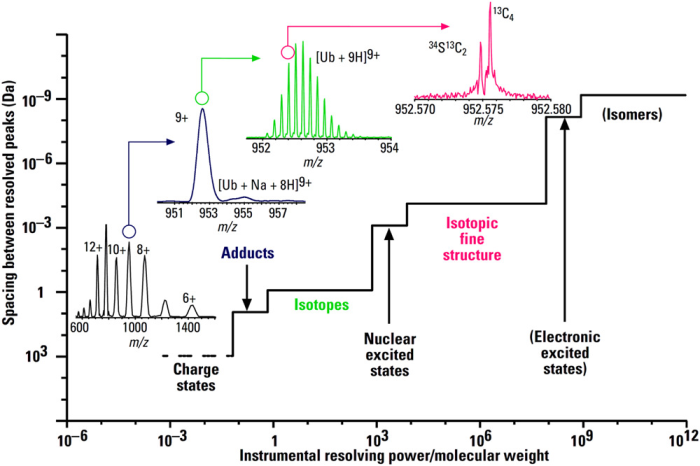
确定质谱特征的元素组成要求仪器能够解析同位素。
最低要求是在目标
m/z
范围内提供单位质量分辨率,或
1/δm > 1
,如图
1
所示。
在高
m/z
范围内,这种分辨能力可以区分初级离子
(
即电离离子,如质子、钠离子等
)
、同位素、修饰
(
即翻译后修饰
[PTMs]
或标记
)
、微小的结构变异或与小分子相关的复合物。
然而,为了实现独特的元素成分分配,所需的
MRP
要高得多
(
即
1/δm > 100)
。
我们将在下文重点介绍
HRMS
在
m/z
范围内实现
10000
左右
MRP
的关键技术。
傅立叶变换(FT)和飞行时间(TOF)质谱是满足高m/z范围(MRP > 10000和m/z > 10000)中高MRP标准的两个主要质谱仪类别。
离子回旋共振(ICR)和轨道阱(Orbitrap)质量分析器是FTMS系列的主要成员,而TOFMS系列由几个变体组成,包括线性分析仪、反射分析仪和多反射/多转分析仪。
大多数FT和许多TOF质谱仪都是混合仪器,前面有四极杆质量过滤器(即Q-TOFMS),便于串联MS分析。
本文不讨论磁质谱,因为它们主要用于低质量数化合物的检测,尽管它们也提供较高的MRP。
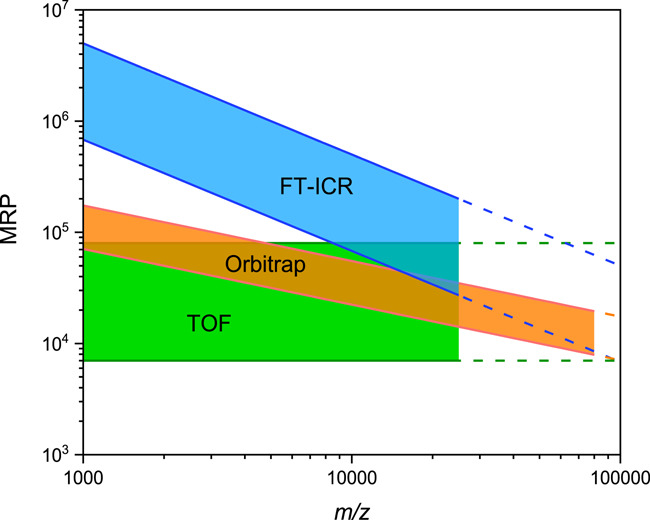
大多数质谱仪的MRP随着m/z的增加而下降。
例如,傅里叶变换离子回旋共振质谱(FT-ICRMS)的MRP随着m/z的增加而线性降低,而Orbitrap-MS的MRP与m/z平方根的倒数成比例。
因此,尽管Orbitrap在m/z= 200时提供了140000的MRP,但在m/z在10000的范围内时,MRP会降低到16000。
TOFMS与上述质谱仪呈现的规律不同,其MRP独立于m/z或在特定条件下随着m/z的增加而逐渐增加。
图2显示了基于MRP的商业化质谱仪的经验规律。
在过去的十年中,这些技术的最大MRP已经有了相当大的进步,研究人员将这些仪器的MRP推向了另一个高度。
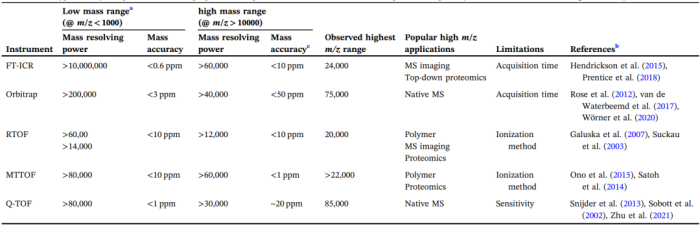
表1总结了重要的商业化HRMS或其改进版本的分析特性,这些特性决定了仪器在高m/z范围内的适用性。
我们还列出了制造商报告的低质量范围(m/z < 1000)商用质谱仪的性能规格,以供比较。
值得注意的是,仪器的MRP是否足以分辨峰还取决于离子的电荷状态(即使用ESI或MALDI生成的离子)。
这些曲线是根据文献报道和仪器制造商提供的数据绘制的。
表1 可用于分析高m/z的通用HRMS的重要典型分析性能和特性
a这里列举了质谱公司提供的低质量范围(m/z<1000)的质量准确度和MRP以供参考;
b FT-ICR、Orbitrap和Q-TOF使用的是ESI,而QTOF和MTTOF类别下的结果是使用MALDI;
1、傅里叶变换离子回旋共振质谱(FT-ICRMS)
FT-ICR质谱仪能根据离子在均匀磁场中的回旋频率分析离子的m/z。
在这种技术中,离子通常在超导磁体的磁场边缘之外产生,并在真空下转移到ICR碰撞池中。
该元件通常是安装在强磁场区的圆柱形彭宁离子阱。
在该单元中,离子在径向上受到洛伦兹力的限制,在轴向上受到捕获电势(VT)的限制。
离子的回旋频率取决于m/z,m/z可以从ICR碰撞池的一对检测板上感应的离子镜像电流得到。
FT-ICRMS(和Oribitrap-MS)呈现高MRP的关键特征是通过非破坏性离子检测方法获得的长时域瞬态。
FT-ICRMS中的典型瞬态长度为0.1–10 s。
人们能观察到的瞬态很复杂,因为它混合了细胞中每个离子的信号。
区分源自不同m/z的信号是通过将时域信号转换成频域频谱的傅立叶变换来实现的,因为更长的瞬态会产生更高的MRP,所以ICR碰撞池需要在超高真空条件(10
9
–10
11
mbar)下运行,以最大限度地减少离子中性粒子与残余气体分子的碰撞。
Comisaro和Marshall等人于1974年开发了FT-ICRMS。
它能提供所有质谱仪中最高的MRP。
最新的商用FT-ICR质谱仪使用动态协调的ICR碰撞池,可以在低质量范围内提供超过10000000的MRP。
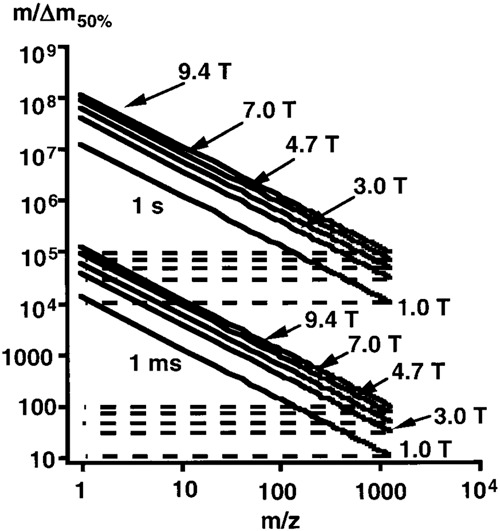
然而,高质量范围内的傅里叶变换ICR质谱仪的MRP下降,如图3所示。
图3 在不同的磁场强度和瞬态长度下,FT-ICRMS的MRP是m/z的函数
FT-ICRMS分析高m/z离子的挑战是多方面的。
第一个限制是离子源和ICR碰撞池之间的离子转移、操作系统的效率和质量工作范围。
在使用射频(RF)电场操作的组件中也会出现这种限制,尤其是在存在强磁场的情况下。
因此,选择合适的离子转移系统是高质量检测的先决条件,例如需要分别降低和增加其RF频率和振幅。
第二个限制是用于分析大质量离子的ICR碰撞池的固有特性。
ICR室中可用于分析的离子理论临界质量(m
c
)或质量上限为:
其中q是离子电荷,B是磁场强度,a是碰撞池的轴向尺寸,α是碰撞池的几何因子。
也就是说,扩展ICR的工作范围可以通过增加磁场强度、增加ICR碰撞池尺寸/降低捕获电势来实现。
在保持磁场稳定性的同时增加磁场强度是ICR技术中的一个主要挑战。
目前最高的ICR磁场大
小是21特斯拉。
由于磁体孔尺寸的限制,ICR碰撞池的尺寸也受到可用磁体的限制,以获得足够的场强和均匀性。
在这种固有的限制下以及在分析之前,人们通过用脉冲氦气以及电场进行碰撞冷却来使离子螺旋化以降低离子的动能,这种方式既方便又有效。
离子运动的冷却可以允许离子阱使用较低的VT并增加信号强度,从而增加质量范围和MRP。
其他方面的进展还包括ICR碰撞池的设计和操作方法。
如前所述,FT-ICRMS的另一个限制是MRP随m/z的增加而线性下降。
这种趋势是由于随着m/z的增加,在相同的瞬态长度内完整循环的数量减少,使得回旋频率的测定不太准确。
为了在高m/z范围内保持高分辨率,人们选择直接扩展瞬态长度;
但对于高质量离子,这会大大增加每次扫描的数据采集时间并降低测量速度,使其与串联质谱中的色谱系统不兼容。
在高m/z范围内导致MRP下降的其他一般因素包括与回旋运动耦合的磁管运动的干扰,以及与残余气体的离子-分子碰撞,这些因素会改变离子瞬态长度和形状。
在轨道阱质量分析器中,被捕获的离子存在于Kingdon trap电极产生的静电场中,Kingdon trap由纺锤状的内部电极和一个的桶状外部电极组成。
为了使用轨道阱进行最佳的分析,我们需要精确控制进入轨道阱的离子角度、位置以及角度和速度分布。
弯曲线性阱(C-trap)会将碰撞冷却离子的脉冲传输至轨道阱中。
在超高真空度(8×10
10
mbar)的环境中,离子沿z轴振荡产生的电流在时域中通过傅里叶变换转换到频域。
谐波轴向振荡的频率与m/z的平方根成反比。
作为FTMS系列的一员,Orbitrap与FTICR质量分析仪不同,Orbitrap质量分析仪无需液氦冷却的超导磁体和额外的磁体组件即可运行,具有相对经济高效和易于维护的特点,不会损害离子的超高MRP和质量准确度。
然而与FTICR不同的是,Orbitrap MS中离子的激发需要在轨道阱外进行,因为阱内碎裂会导致离子损失。
首个商业化的Orbitrap于2005年推出(Thermo Fisher Scientific)。
2011年Thermo Fisher Scientific发布了一款全新的高强度电场Orbitrap,这款Orbitrap采用了增强型的傅里叶变换算法,将MRP提高了四倍。
2012年,人们将质量范围扩展至m/z =24000以改进了对完整大分子的分析性能(集成了高能碰撞诱导解离[HCD]室的Exactive Plus Orbitrap)。
简而言之,人们引入了一种经过改进的RF电路,使得所有多极RF中的RF频率更低,包括C-trap。
高气压充氙的HCD室内可以实施更有效的去溶剂化和碰撞冷却,这增强了对蛋白质分子的检测灵敏度。
人们在该模型中检测到了GroEL离子,一种800.8 kDa的同源寡聚蛋白质复合物。
在m/z为10000至1000时,离子峰的MRP和质量误差范围约为4000和< 20 ppm。
为了满足人们对生物大分子的结构、功能和相互作用进行表征的需求,研究人员将可检测的m/z范围扩展了3至4倍,并做了进一步改进。
在该模型中,RF对离子导向频率的限制进一步降低,以增加高m/z的传输。
加合物消除不足和从大气压转移到真空期间离子获得的动量分别导致MRP的下降和灵敏度损失。
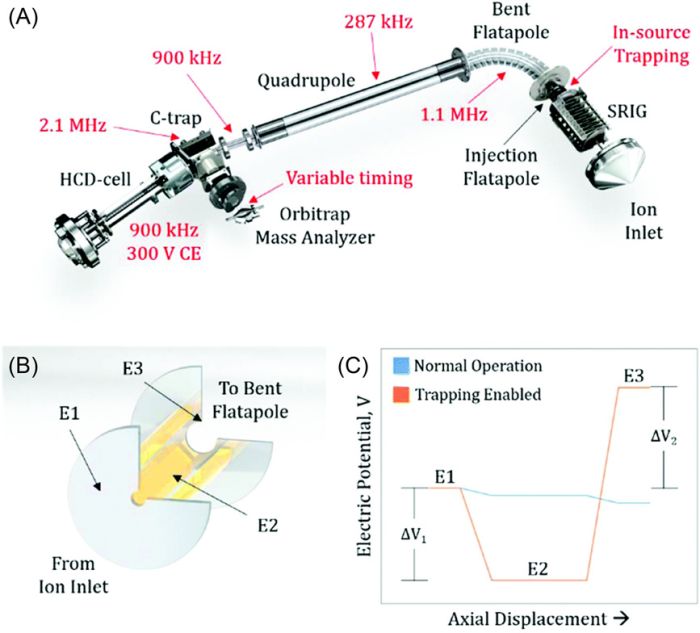
如图4所示,人们对质谱的injection flatapole进行了改进,实现了源内离子的捕获,从而实现了更有效的去溶剂化和动量降低。
人们通过降低偏转电极上的脉冲转换速率,优化了高质量离子从C-trap到Orbitrap的传输过程。
总的来说,这个过程离子丰度提高了5-10倍。
在这种情况下,由于更有效的离子传输,质谱通常在几分钟范围内完成数据统计。
通过这些修饰,人们可以检测到大约75000的m/z(乙型肝炎病毒核衣壳组装),这是迄今为止在Orbitrap质量分析仪中检测到的最高m/z。
m/z约为25000时,平均质量误差在3 ppm以内,m/z为400时,MRP高达200000。
理论上,m/z为10000时,MRP为40000,采集时间相同;
然而,人们仅报告了m/z > 10000的低分辨率数据。
最近的一项研究表明,在基于Orbitrap的单粒子电荷检测(CD)技术中,人们通过在低离子计数条件下确定了大量单个离子的电荷和接近理论预测的高MRP,而这一方法以更长的采集时间作为代价。
关于大分子检测中其它电荷检测质谱法(CDMS)细节的文章可以在别处找到,这里不做赘述。
图4 在Orbitrap质谱仪上实施源内离子捕获以提高高质量结构分析能力的示意图
A,仪器的修改用红色标明;B,传输平台的示意图;C,正常/源内离子捕获模式中的相对电位。该仪器实现了更有效的去溶剂化和碰撞冷却,从而提高了MRP和质量传输效率。
FTMS需要复杂的长时间镜像电流瞬态测量(通常从几秒到几分钟)来获得大蛋白质的同位素分辨率,这对高通量分析是不利的。
然而,高分辨率并不总是必要的,也就是说,电荷状态的分化需要比识别细微PTM分化(例如磷酸化)相对更低的MRP。
此外,仪器需要保持超高的真空度,以确保振荡离子有足够的平均自由程;
或者,TOFMS是另一种通用的选择。
关于高扫描速度和自由空间电荷效应,我们将在下一节讨论。
飞行时间质谱仪根据离子飞越无磁场区域的时间来分析离子,由此可以推断出它们的m/z。
在为离子提供势能(qU,其中U是离子源的电势)的电场下,离子源区域会产生离子。
在离子产生之后,离子被抽出并加速到封闭在飞行管内的无场区域。
加速过程将离子的势能转化为进入无场区域前的动能()。
在无场区域内,不同m/z的离子表现出不同的速度。
飞行时间(t)和离子质量(m)之间的简化关系为:
其中L为无场区域的长度。
在TOFMS中,MRP可以转换为时间t/(2Δt)。
由于t随L呈线性变化,因此目前的共识是原则上飞行管长度越长,MRP越高。
根据定义,降低Δt可以实现更高的MRP。
为了在飞行时间质谱中获得较高的MRP,电离时离子的能量和空间扩散需要最小化。
值得注意的是,能量扩散随着离子m/z的增加而增加。
提高飞行时间质谱仪MRP的两个最重要的技术是离子延迟引出和反射器技术。
离子延迟引出在Wiley和McLaren (1955)介绍的两级离子源中完成。
这种离子源的第一阶段是电离发生。
电离后,离子被引出,并被一个温和的电场推向第二阶段。
第二阶段用强电场将离子加速到它们朝向无场区域飞行的最终速度。
当进入无场区域时,不同m/z的离子通过它们到达检测器表面的时间而被分离。
延迟引出是在电离后的第一级施加较短的延迟电压,延迟范围在几十纳秒到低微秒之间的一种方法。
它有效地最小化了离子的初始能量扩散对到达时间的影响。
另一方面,反射器使用飞行管中的环形电极堆来产生电场,以反射离子的轨迹。
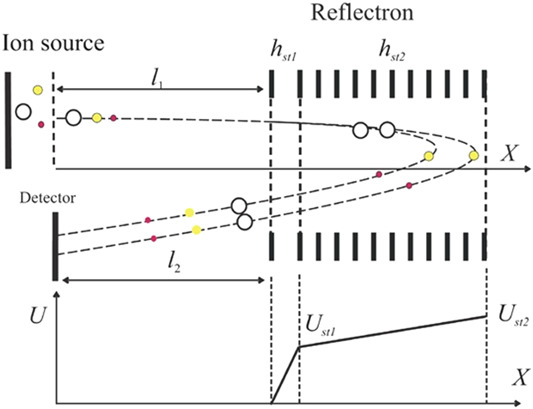
反射器可以进一步补偿离子在反射过程中的能量差异,因为初始能量较高的离子会在反射器中传输更深,而初始能量较低的离子会传输更浅,如图5所示。
通过适当选择反射器后的飞行距离,具有相同m/z但不同初始能量的离子将同时到达探测器,实现飞行时间聚焦效果。
使用反射器的另一个优点是飞行距离的增加,这可以增加t和MRP。
具有较高动能的离子在反射器中穿透得更深,促进了检测器的聚焦效果。
自20世纪60年代以来,TOFMS一直是最受欢迎的技术之一。
在线性飞行时间质谱仪中,基本上不存在质量上限,因为离子经过电势加速后会沿着直线向检测器传输。
由于离子运动不受射频电场的控制,轨迹与m/z无关,常规线性模式飞行时间质量分析仪可以检测MDa水平的离子(即使用专用的基质分子,电荷检测器,或专门的低温离子探测器,如下所述),尽管其灵敏度和MRP都没有完全优化。
为了获得高分辨率光谱图,典型的TOF质谱仪是在反射模式下运行的,在低质量范围内提供大约10000–60000的MRP。
尽管其MRP在大多数质量范围内低于FTMS,但TOFMS的扫描速度比FTMS快2-3个数量级,可完美匹配联用分析系统。
TOFMS中有几个变化进一步增强了MRP。
最有吸引力的解决方案是安装静电扇区或多个反射器,以增加飞行距离。
一个例子是多圈或螺旋飞行时间质谱仪,它可以很容易地将飞行距离延长到几十米以上。
对于m/z约为10000的离子,这种仪器的最大MRP超过20000。
虽然飞行时间质谱基本上没有质量上限,但最大可观测m/z仍然受到一些关键因素的限制,包括样品制备、电离、离子轨迹、检测器特性等。
这种仪器方面的限制主要是指用于检测大分子的离子检测器的灵敏度。
例如,传统微通道板(MCP)检测器的灵敏度随着离子速度的降低而降低。
由于较高的m/z离子表现出较低的速度,这种检测器对于大分子分析是低效的。
为了克服这一问题,其中一个有效的解决方案是用更灵敏的替代物取代MCP检测器,例如通过能量感应撞击离子的能量敏感型低温检测器。
低温检测器可以将飞行时间质谱的质量上限提高到大约2 MDa。
低温探测器的缺点是响应时间长,通常在微秒范围内,这会导致较高的δt产生。
响应时间比传统的MCPs长两个数量级以上,无法产生高分辨率的质谱图。
TOFMS的另一个不可避免的问题是检测器偏向于检测低质量的离子,该问题主要是由于低质量离子导致的检测器饱和所致。
这种偏差源于MCP检测器在离子撞击表面后恢复其离子记录能力所需的时间。
在恢复时间窗口内,同一检测器区域的离子传输受到阻碍。
由于质谱通常存在低m/z的杂质离子,这些杂质离子可能是与基质相关的分子或较大离子的碎片,因此对高m/z离子的灵敏度要低得多。
人们可以通过改变检测器电压来调整增益效果,从而降低偏好程度;
也可以通过离子或检测器门控来使该问题最小化,以保持检测器在高m/z范围内的灵敏度。
有一种动态仪器优化方法被证明可以将灵敏度提高2-3倍。
TOFMS的另一个限制是,质谱仪存在离子损失现象,反射器不适合分析高m/z离子。
这种损失可能是由于离子在进入反射器之前在飞行管中的亚稳态衰减,因此它们在不同的时间到达检测器。
反射器的另一个可能的问题是较高的m/z离子具有较宽的发散角,使得离子轨迹在反射后偏离检测器轴。
为了进行高m/z离子的检测,人们通常通过商用化的TOF仪以线性模式进行实验,但这不可避免地会降低光谱的MRP。
人们发展了一种综合的计算方法来预测线性飞行时间质谱仪的最终构型,这表明离子源区域的尺寸以及引出电压和延迟的组合在MRP的改进中起着关键作用。
串联质谱(MS
n
)是一种技术,该技术在概念上集成了两个或多个质量分析器,可以提高质谱破译复杂化合物信息的能力。
最初开发于20世纪80年代初的四极杆-飞行时间(Q-TOF) MS已成为高分辨率和高质量应用中最常见的混合仪器之一。
四极质量分析器包括四个平行的双曲线或圆柱形杆状电极,并通过调节直流(DC)电压和RF电压的频率和幅度来传输或存储特定m/z的离子。
四极质量分析器通常设计紧凑,且需要低真空,并且具有很高的离子容量。
四极杆质量分析仪兼容各种电离技术(如ESI和MALDI)以及离子激活方法(例如电子激活解离和光诱导解离)。
四极杆质量分析器的主要缺点包括对离子传输、质量检测范围和质量分辨能力(通常为单位质量分辨率)的限制。
混合Q-TOFMS得到了广泛的认可,因为它保留了双方的优点(分别是选择性和高MRP ),而没有增加缺点。
离子传输效率的提高使得在Q-TOFMS中检测大分子化合物成为可能。
根据RF频率和振幅以及杆组件的直径,传统的四极杆质量分析仪可以在高达4000的有限m/z下运行。
Q-TOFMS通过增加四极杆区内的压力进而促进对大分子径向运动的碰撞冷却,导致了离子传输效率的提高。
Q-TOFMS通过将四极杆的射频频率降低至300 kHz,实现了更宽的m/z范围至40000(一种蛋白质复合物,m/z为38150的GroEL伴侣蛋白)。
在这种情况下,不同的真空泵保持着高压,包括紧挨在取样锥后面的一个室(10 mbar)、六极周围的一个金属套筒(局部压力为8×10
3
mbar)和一个碰撞室(1.5×10
2
mbar)。
正交TOF区域中的离子传输效率也通过在离子透镜上使用低计数网格和较低重复率的离子反射器(即加速前的传输时间为410 μs)而得到提高。
可检测的m/z超过85000(碘化铯簇),在m/z约为84000时信噪比(SNR)为5。
在串联MS模式下,四极杆具有窄带质量过滤器,因此只有窄m/z范围内的(前体)离子被传输到TOF区域,从而提高了检测动态范围和信噪比。
理论上,四极杆质量分析仪传输的离子比设定值高4-5倍:
将离子传输的m/z设置为32000应传输m/z为128000-160000的离子。
随着电离和检测效率的进一步提高,Q-TOFMS可以继续检测超过90000的m/z离子。
此外,在Q-TOF质谱仪中,离子光学已得到改进,以实现更好的MRP以及质量相关传输。
低温度系数陶瓷垫片的使用可以减少温度引起的质量漂移,该瓷片可以利用对称屏蔽对所有电极进行更好的离子聚焦;
与之前的模型相比,MRP提高了约35%。
离子从四极杆通过正交TOF转移至检测器,这进一步改变了离子光学设计理念。
更详细地说, “步进式转移时间”可以调整不同m/z的离子从碰撞单元行进到正交加速单元的时间。
使用较大的入口孔径和较高的加速场,探测效率提高了30%。
最近,离子淌度谱(IMS)是一种集成到飞行时间质谱中的一种技术。
IMS的加入为大分子分析提供了另一个分离维度,在电场的影响以及缓冲气体的存在下,具有不同迁移率或平均碰撞横截面的离子根据不同的淌度信息被分离开。
与四极杆质量分析仪类似,离子淌度池具有减少能量分布、降低化学噪音、提高检测动态范围和传导MS
n
的优势。
IMS的各种设计,例如行波离子迁移谱(TWIMS)、捕集离子迁移谱(TIMS)和环形离子淌度(cIM),都被证明可以增强淌度分离和离子传输。
首个市售的IMS-Q-TOFMS于2006年推出(Waters,Synapt high definition MS[HDMS])。含有TW堆叠环形离子导向器的离子淌度池取代了六极杆,有效地将离子从离子源区域桥接至四极杆质量分析器,并消除了不需要的中性物质。在该系统中,位于四极杆和正交TOF之间的“TRIWAVE”系统(捕集、IM和转移池)不仅能实现淌度分离,还能激活离子,因此有利于定量结构分析。TIMS的工作原理是通过使用电场推动离子与逆流的中性漂移气体分子不断碰撞,从而分离离子。TIMS质谱于2016年才商业化,并因其对天然大分子组装体的结构解析能力而广受欢迎。现代的IMS-Q-TOFMS可以在m/z 10000以上提供平均50000的MRP
。
由于数据复杂性和分析要求的增加,数据处理是HRMS的另一个重要部分。
与仪器的重大发展相反,数据处理可能是提高数据质量的一种有效而方便的手段。
在傅立叶变换质谱(FTMS)中,数据处理尤为重要,因为在傅里叶变换之前对原始数据进行校正、滤波和变迹是获得谱图的常见做法。
例如,人们发现相位校正可以显著提高FT-ICRMS的光谱质量,包括SNR、MRP和质量准确度。
在其他质谱数据中,离线或采集后处理提高了分子鉴定的谱图质量。
例如,人们可以通过波变换、翘曲函数以及其他方法提高峰值检测和降噪的效率。
研究表明,充分的校准可以将质量准确度提高一个数量级以上。
另一方面,采集后数据校准可以通过比较多个光谱以自校准方式进行。
复杂光谱中蛋白质的鉴定也可以通过使用多峰拟合和模拟技术提高蛋白含量来实现。
相比之下,人们通过使用简单的峰对齐算法(而不是使用复杂的校准函数),就可以实现在线的自校准。

(4).jpg?x-oss-process=image/resize,m_pad,w_80,h_60,color_eeeeee)





加载更多