溶剂效应——如何消除色谱峰这个隐形“杀手”???
溶剂效应指稀释剂溶剂强度大于流动相时造成色谱峰变形的现象。如用THF溶解样品,注入流动相为乙腈-水(18:82)的反相系统中,可能会造成峰分叉或拖尾的结果,还会导致保留时间漂移。
表现为液相色谱上较早洗脱的峰前沿或分叉(也有可能表现为肩峰),较晚洗脱的峰则较为正常。也可能全部峰均出现分叉的情况,视溶剂强度而定。
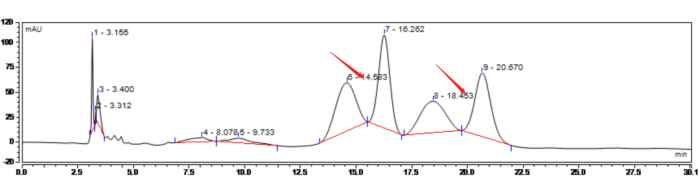
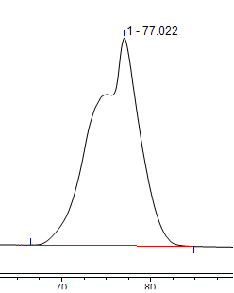
在分析某手性样品时因溶剂效应产生的两个分叉峰
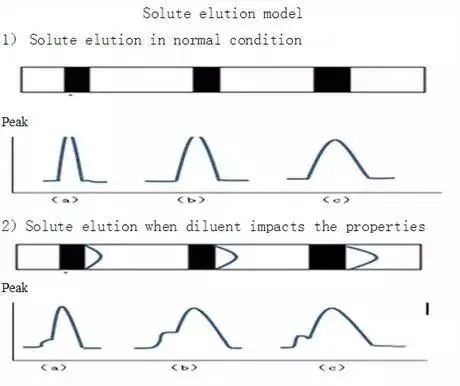
第一阶段:样品刚被注入系统,进入 后,流动相氛围中的目标物以正常速度被洗脱。因强溶剂洗脱,移动速度快,样品在空间上开始慢慢分裂。
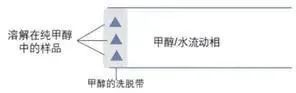
第二阶段:在一定时间内,溶剂氛围中的目标物移动始终快一些,前后两部分距离扩大。但移动快的目标物所处氛围逐渐被流动相稀释(注:因为溶剂和流动相均不保留),其移动速度会逐渐降至正常流速。直到前面目标物的氛围完全被流动相替代,前后两部分的距离稳定下来。因而,样品溶剂与流动相洗脱强度差距越大,两部分目标物最终的距离拉的越大。
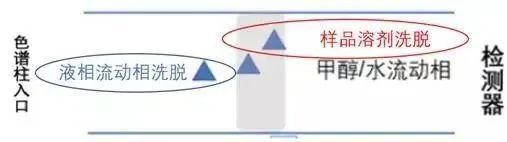
第三阶段:所有目标物在 中正常移动,但分裂已不可逆转。

经过检测器,同一目标物给出了两个色谱峰。其中进柱前即扩散进入流动相的那部分目标物组成了后面的色谱峰,它的保留时间与目标物的真实保留时间基本吻合。
简单概括,强洗脱溶剂不均衡地参与了目标物的洗脱,使色谱峰保留时间整体提前,而样品在柱前的不充分扩散导致了峰形扭曲。这种影响轻则导致峰展宽,严重时甚至导致峰裂分,给定性定量带来灾难。
反相色谱系统中溶剂强度的顺序为:
水(最弱)<甲醇<乙腈<乙醇<四氢呋喃<丙醇<二氯甲烷(最强)
正相色谱系统溶剂强度顺序为:
正己烷(最弱)<醇/正己烷混合<乙醇<四氢呋喃
溶解样品的溶剂强度大于该样品出峰时流动相强度,样品溶剂可以看成流动相的一部分,一部分样品溶解于溶剂中会被迅速洗脱出 ,而一部分样品溶解于流动相,被流动相洗脱出,这样会造成色谱峰的展宽或者分叉。
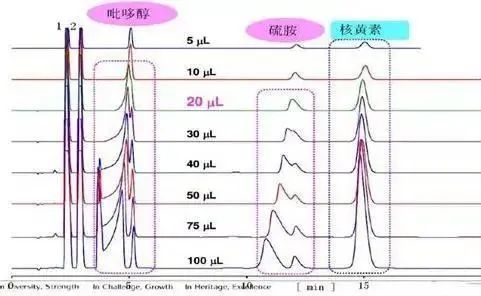
当进样体积较小时,扩散至流动相中的溶质占大多数,且扩散在很短时间内完成,因此峰形与用流动相直接溶解样品无大差异。随着进样的体积增大,留在溶剂本身里的溶质的量逐渐增大,当进样体积增大到一定数量,留在溶剂里的溶质的量变得不可忽略,在色谱图上就表现为色谱峰的分叉、拖尾等。
有时,当我们使用流动相或流动相中的有机相无法直接溶解样品,这时很多小伙伴会选择使用氯仿、甲苯等能溶的溶剂,甚至DMSO这样的“万能溶剂”来溶解样品。这样进样的结果是溶剂与流动相不兼容,溶质难以在流动相中扩散。
又如,在做参比制剂的溶出曲线中,溶媒中经常加入表面活性剂。而带有表面活性剂的溶剂进样后,由于溶质在含有表面活性剂的溶剂中的分配系数与在流动相中的分配系数存在较大差异,就会导致峰形的问题,甚至保留时间的漂移。
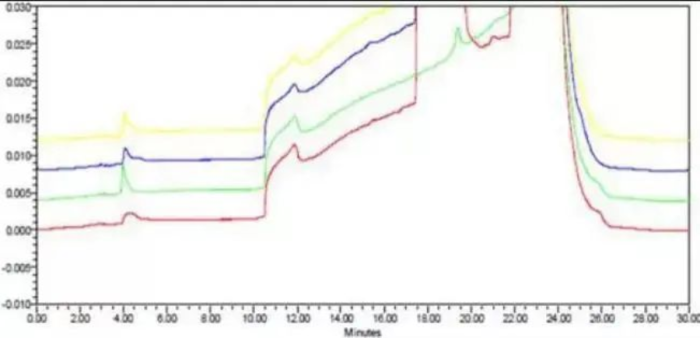
电离状态的差异主要由溶剂和流动相各自的pH差异引起。我们都知道,在反相体系中,目标化合物的存在状态不同,保留行为会有明显的差异,而存在状态就取决于目标化合物在不同pH体系内的电离状态。若样品在溶剂和流动相中电离状态差异较大,样品溶液在接触流动相的过程中,来不及缓冲至流动相中的电离状态,这个时间如果较长,就容易表现为保留时间发生错位或峰形变形,如下图的案例。
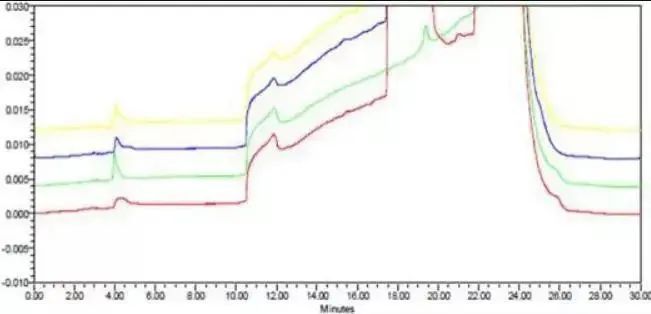
流动相为pH 3.0缓冲盐。绿色谱图为对照品,另外三个谱图样品的溶剂从下至上分别为0.1%磷酸、纯化水、pH 3.0流动相
柱前管路内径越大、管路越长,越利于目标物向流动相扩散,而且使用更粗的管路比更长的管路有效(注:假设死体积相同)。虽然粗的管路加剧了等度条件下的柱外展宽,对柱效有危害,然而相较于峰分叉的危害而言,前者尚能接受。
这就是为什么有时候会发现,HPLC的液相(管路死体积大)比UPLC的液相(管路死体积小)色谱峰型好。
1.导致柱效下降,影响分离。
2.影响峰形,甚至影响定量、定性结果。比如,在LCMS中,扫描前体离子时,遇到这种情况,甚至不知道哪个峰才是目标物。
3.当标样和样品的溶剂不一致时,保留时间不吻合,同样影响定性。如酒类成分分析,标样溶于纯水,样品是过滤的酒,后者的溶剂就是乙醇水,它的保留时间必定早于纯水溶解的标样;再比如水中污染物分析,目标物溶于有机相得到标样,而样品是过滤后的天然水;
4.强洗脱的溶剂在基质中提取出的杂质遇流动相会析出,堵塞针座、柱前管路或 。
调整稀释剂或流动相,使二者洗脱能力接近,或稀释剂洗脱能力稍低于流动相。
一般情况下,为避免溶剂强度差异导致的溶剂效应,反相色谱中较为稳妥的做法是稀释剂中有机相比例和流动相相当,必要时可略高于流动相,但应当据其评估其溶剂效应风险。
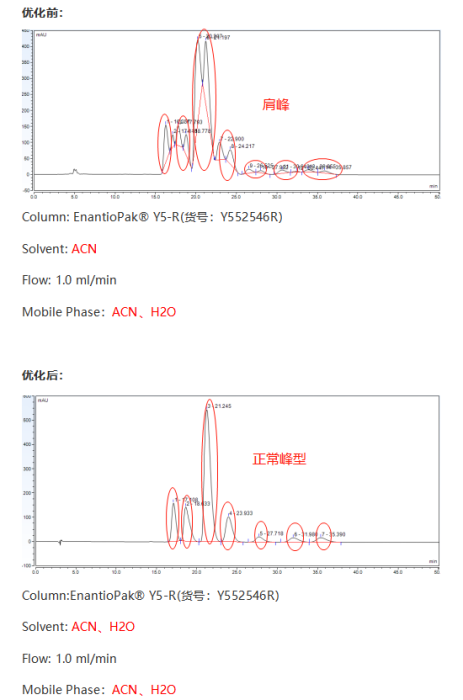
如下图,我们在分析手性化合物时发现所有主峰均出现肩峰(或分叉峰),这种情况很容易考虑没拆开。但所有主峰都分叉的现象在手性化合物分析中是非常罕见的,考虑溶剂效应后,用流动相溶解样品后,肩峰消失。
为保证峰形,进样体积一般控制在5-20μL,尽量不超过25μL。
如不能减少至合适的进样体积,应尽量选择与流动相比例相同或接近的溶剂。
使溶剂与流动相有较好兼容,目前办法有两个:
a. 若流动相或流动相中的有机相无法直接溶解样品,则用可以溶解样品的溶剂溶解成高浓度储备液,然后用流动相稀释至所需浓度。
b. 在流动相中加入同样的助溶剂或表面活性剂,或提高有机相的比例。
电离状态的差异许多情况下会表现为保留时间的漂移或不稳定。可以通过将样品溶液的pH调节至与流动相一致,或增大流动相的缓冲能力来改善。
若采用梯度洗脱,在不影响分离度的情况下,可以改用较粗内径的柱前管路。但此法不适用于等度洗脱,会降低柱效。
药物分析学社
展源
何发
相关文章
-

如何避免溶剂效应?
2021-07-25
-

【干货】如何避免溶剂效应
2022-02-09
-

溶剂效应是怎么回事?
2024-02-29
-

如何完美解决“溶剂效应”?
2022-08-04
-

如何完美解决“溶剂效应”?
2024-04-29
-

助焊剂的活性成分、溶剂等组成及研究进展
2020-05-27
-

液相分析过程中如何避免溶剂效应?
2023-04-18
-

【划重点】如何解决“溶剂效应”?
2025-03-19
-

反相色谱中溶剂效应的原理及解决方法
2023-02-20
-

液相分析过程中“溶剂效应”的那些事儿~
2023-06-16

加载更多