测定I、II、III类残留溶剂
测定I、II、III类残留溶剂
药物中的残留溶剂是指在药物活性成分、辅料及加工过程中使用的,但未能在净化过程中完全去除的溶剂。对于残留溶剂应尽可能地去除,使之符合ICH(人用药品注册技术要求国际协调会)指南的要求。本文介绍了应用压力平衡顶空系统,高效、精确地测定I、II和III类药品残留溶剂的方法。
药品生产过程中常常会使用大量溶剂,其中一些溶剂能决定药品的特征(如晶形态、纯度和溶解性能等),是药品合成的关键。ICH和美国药典(USP)都制定了相应的条例限制药品中溶剂的使用量,其中ICH列出了3类对人体和环境有毒害的溶剂。直至2008年,USP限制和测定的溶剂仅有三氯甲烷、二氧六环、二氯甲烷和三氯乙烯。为与ICH保持一致,USP修改了第467章的内容,其中包含I、II、III类溶剂的全部清单、控制限量以及各溶剂鉴定、确证和定量的相关程序。
修订版建议采用配有火焰离子化检测器(FID)和自动顶空进样器(HS)的气相色谱仪(GC)分析残留溶剂,并将测试样品的溶剂残留分为3个步骤:样品筛查及鉴定(程序A)、确证(程序B)和定量测定(程序C)。本文应用压力平衡的顶空进样系统,将样品引入GC-FID来分析I、II、III?这3类溶剂的残留。
试验
仪器设备:配有FID检测器和顶空进样系统(TurboMatrix HS-40)的Clarus 600 GC。TurboMatrix HS-40是基于压力平衡的进样系统,样品采集量根据已知流速的气体在一定时间内进入分析柱的体积来计算。与其他顶空技术相比,该系统精密度高、操作简单且管路惰性化处理。不需要气体进样阀和其他活动部件,既减少了样品与热金属样品环接触,又无需维护活动部件。系统包括多位样品炉,该样品炉具有重叠样品瓶加热的功能,一旦GC温箱准备好,第2个样品即可进样,因此其样品通量非常高,操作条件见表1。
建立在高通量顶空系统基础上,Clarus600 GC具有优于同类产品的降温速度,减少了样品运行结束与下一样品进样之间的时间,具体操作条件见表2。
讨论
本文分析了列表中的所有溶剂,并优化了方法的分辨率和运行时间。第467章中包含的所有溶剂在G16和G43 都获得完全分离。在多维分离时,每一类溶剂都使用了两种稀释剂,稀释剂的选择是方法建立中非常重要的可变因素,同时材料和分析物的溶解性、沸点以及制药公司所使用的溶剂种类等因素均需考虑。每个分析物的响应会随所选稀释剂的改变而改变,因此必须谨慎选择。一些典型的非极性溶剂使用水作为稀释剂时,可以获得良好地响应;但一些极性溶剂则需要使用有机溶剂作为稀释剂。
鉴定和确证残留溶剂
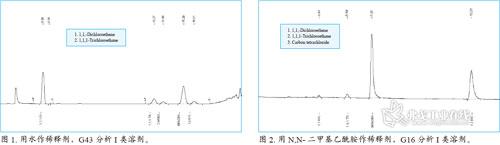
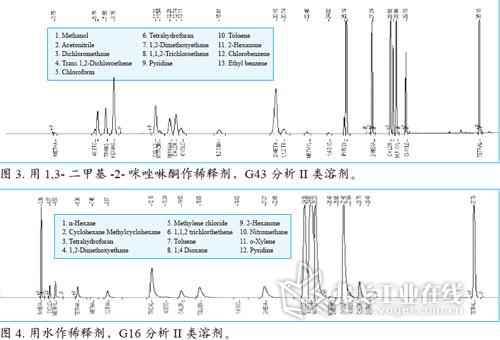
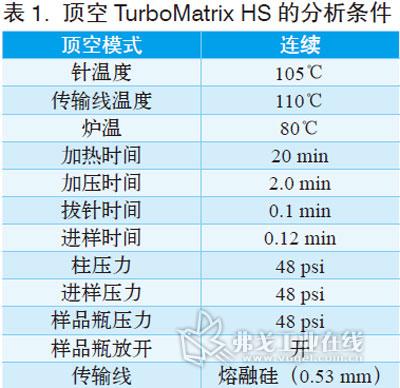
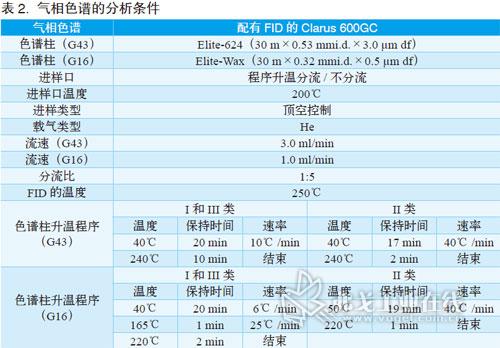
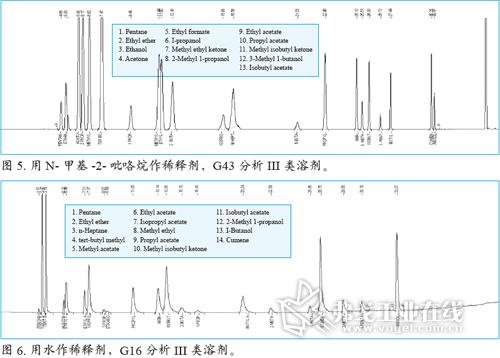
程序A用于鉴定相关药品中的残留溶剂,使用 G43进行初步分析,所得不同稀释剂的谱图见图1、3、5。程序B使用 G16对残留溶剂进行确证。G43和G16的出峰顺序不同,允许分析物在两根正交柱上通过保留时间进行定性。分析物在G16中分离的色谱图见图2、4、6。
定量
通过程序A、B鉴定和确证了相关药品中的残留溶剂后,各分析物在程序C中被定量分析。程序C对样品中残留溶剂的分离条件进行了优化,根据感兴趣的目标分析物的分离条件选择准确的定量方法。
小结
本文介绍了全面鉴定、确证及定量I、II、III类溶剂的分析方法。TurboMatrix HS重叠样品瓶加热的功能使得一旦GC达到开始条件,体系便立即运行下个进样程序。Clarus 600 GC的柱温箱可快速降温,减少了样品间的进样时间间隔,实现了高通量分析。文中列举了典型残留溶剂在G43和G16的两维分离,且根据测试物质的溶解性和最不易挥发溶剂的沸点两方面因素选择了不同的稀释剂,结合 的选择性,可使所有I、II、III类溶剂得以分离。
珀金埃尔默仪器有限公司
展源
何发
热点文章
-
【干货】革兰氏染色的原理、步骤、误区及结果判读!
2025-09-28
-
【干货】如何进行氢氧化钠溶液的标定!
2025-10-14
-
【细看】常见26种试剂的危害与防护!
2025-09-29
-
【必看】 安全分类分级你都了解了吗?
2025-11-17
-
【谨记】 安全“四不”要牢记!
2025-11-10
-
危险源如何辨识?!
2025-09-22
-
紫外杀菌灯的原理、使用及维护
2025-10-31
-
安捷伦在中国:加速本土创新与绿色发展的双重推进
谈及2024年安捷伦大中华区的业绩表现,杨挺表示,尽管在2023年和2024年全球经济增速放缓,安捷伦中国的业绩仍稳步增长,尤其在制药、食品、环境等行业展现出强劲的市场需求。未来,随着中国科技创新和绿色发展政策的持续推进,安捷伦将继续深化在中国的布局,进一步推动本土化创新。 总结 2024年安捷伦媒体沟通会不仅展示了安捷伦在液相色谱领域的创新成果,也体现了公司在中国市场的深耕与战略部署。
作者:张明
-
洞察未来,共谋发展 “ 数·智·未来 ” 安捷伦未来 媒体圆桌会成功举办
-
食品检验理化常用国家标准与要点
-
水分测定方法开发研究&检测相关问题故障分析解决解读
-
药物常用的晶型表征方法









评论
加载更多