全球首个ctDNA检测方案大规模评估数据出炉

▲论文首页截图
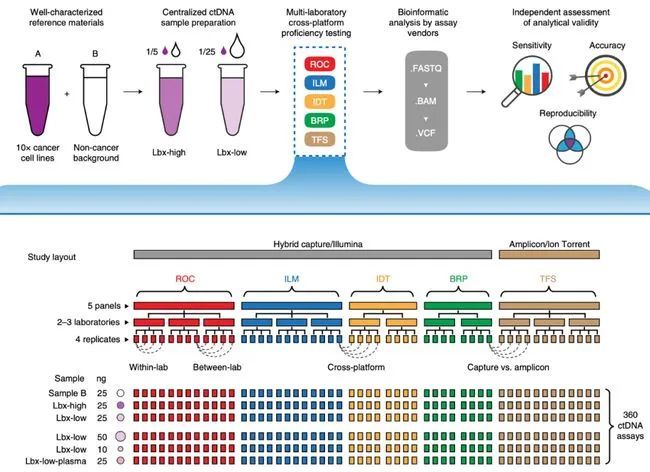
▲实验流程设计逻辑示意图
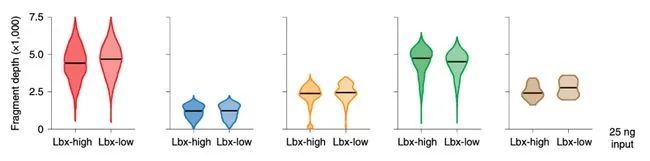 ▲
25ng投入量下有效片段回收率
▲
25ng投入量下有效片段回收率
二是“panel覆盖均一性”,在同样都是25ng的DNA投入量的情况下(相当于7500个基因组拷贝),SEQC2比较了不同panel测序深度对目标设计区域覆盖率的差异,更好的覆盖均一性可以保障即使困难区域也能得到良好的覆盖,从而提升检测的灵敏度。 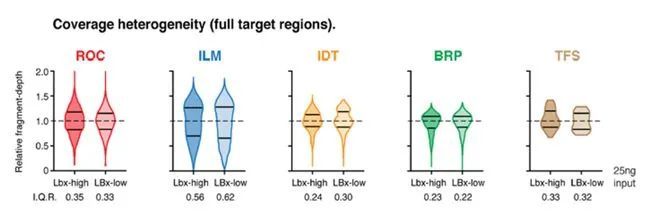
▲液体活检panel覆盖均一性评估
SEQC2通过对每个文库目标区域已知变异的检出结果分析,来评估基于杂交捕获法的ctDNA检测灵敏度。在高频突变中,所有panel都表现出了极高的灵敏度,再次佐证了样本中ctDNA含量对检测结果的重要影响。但在VAF到达0.5%以下的“挑战区”时,不同panel的表现开始呈现显著的差异。其中,低VAF突变中燃石朗清®和xGen Non-small Cell Lung Cancer成为灵敏度最佳的NGS液体活检panel之一:在VAF为0.3-0.5%时,灵敏度>90%。
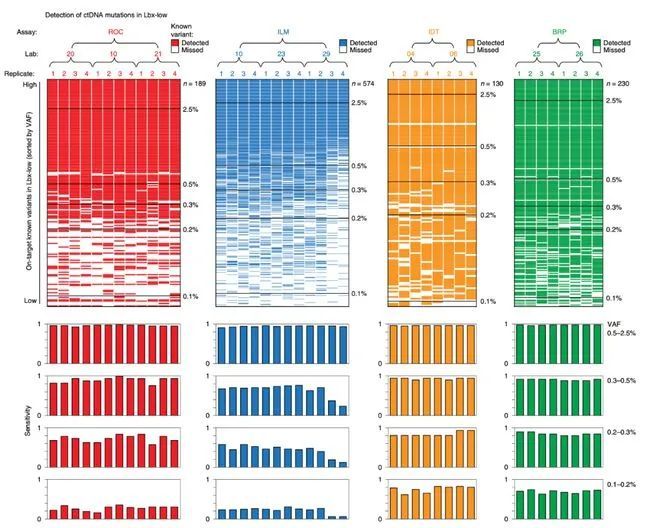 ▲不同VAF对ctDNA检测灵敏度的性能评估
▲不同VAF对ctDNA检测灵敏度的性能评估
而在保证高灵敏度的同时,如何保持低假阳性率,来确保结果的准确性?参与SEQC2的所有panel分析均使用独特的分子标识符(Unique Molecular Identifiers,UMIs)来纠正测序错误,假阳性率相对较低。考虑panel大小后,在25 ng DNA投入量下,燃石医学panel的假阳性率最低(0.03 FP/kb),错误的变异几乎完全发生在VAF<0.5%的区域。综合灵敏度与特异性的整体评估,NGS液体活检panel中燃石朗清®准确性最佳。
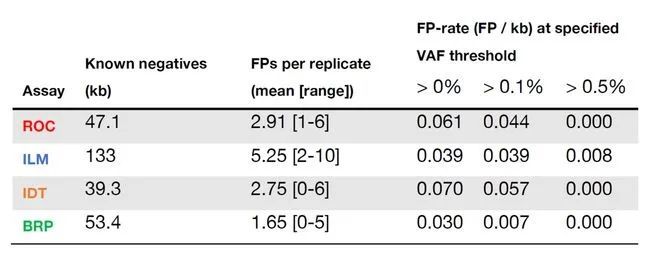
▲25ng DNA投入量时,不同panel 假阳性率表现
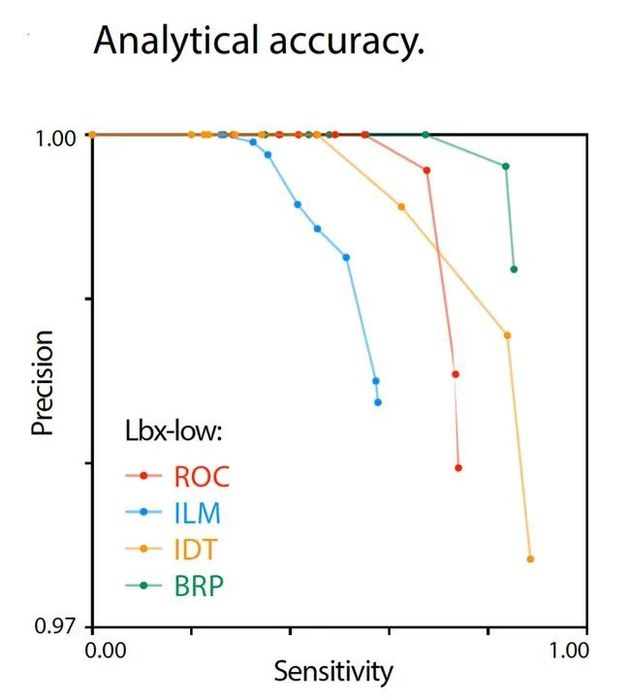
▲25ng DNA投入量时,燃石朗清®的准确性最佳
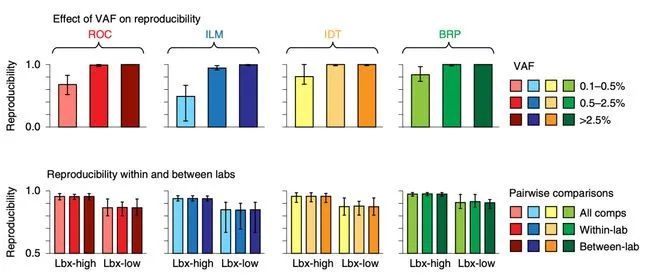
▲实验结果可重复性评估
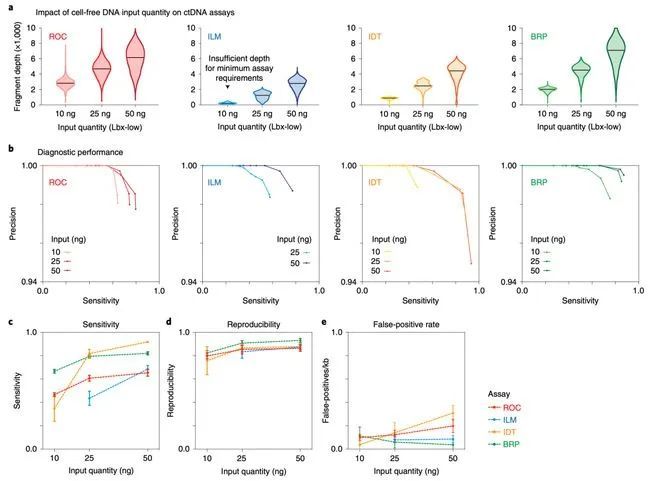
▲不同DNA投入量时对panel性能的综合考量
奇点网
展源
何发
热点文章
-
【干货】革兰氏染色的原理、步骤、误区及结果判读!
2025-09-28
-
【干货】如何进行氢氧化钠溶液的标定!
2025-10-14
-
【细看】常见26种试剂的危害与防护!
2025-09-29
-
【必看】 安全分类分级你都了解了吗?
2025-11-17
-
【谨记】 安全“四不”要牢记!
2025-11-10
-
危险源如何辨识?!
2025-09-22
-
紫外杀菌灯的原理、使用及维护
2025-10-31
-
安捷伦在中国:加速本土创新与绿色发展的双重推进
谈及2024年安捷伦大中华区的业绩表现,杨挺表示,尽管在2023年和2024年全球经济增速放缓,安捷伦中国的业绩仍稳步增长,尤其在制药、食品、环境等行业展现出强劲的市场需求。未来,随着中国科技创新和绿色发展政策的持续推进,安捷伦将继续深化在中国的布局,进一步推动本土化创新。 总结 2024年安捷伦媒体沟通会不仅展示了安捷伦在液相色谱领域的创新成果,也体现了公司在中国市场的深耕与战略部署。
作者:张明
-
洞察未来,共谋发展 “ 数·智·未来 ” 安捷伦未来 媒体圆桌会成功举办
-
食品检验理化常用国家标准与要点
-
水分测定方法开发研究&检测相关问题故障分析解决解读
-
药物常用的晶型表征方法









评论
加载更多